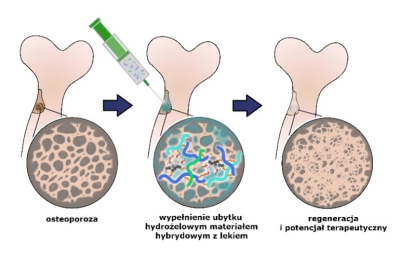
 Zespół w składzie: prof. dr hab. Maria Nowakowska, dr hab. Joanna Lewandowska-Łańcucka oraz dr Adriana Gilarska opracował materiał, który pomoże odbudowywać ubytki kostne i jednocześnie może służyć jako nośnik leków przeciwko osteoporozie dostarczając je wyłącznie w miejsca zmienione chorobowo. Nowy materiał ma postać hydrożelu, który wstrzykuje się w miejsce ubytku kości, gdzie następnie dochodzi do jego „zestalenia” w wyniku sieciowania chemicznego zachodzącego w temperaturze 37°C. Ze względu na swoją strukturę i skład hydrożel trwale przyczepia się do tkanki kostnej i pełni funkcję rusztowania, na którym w naturalnych procesach biologicznych tworzy się nowa tkanka kostna wypełniająca ubytek.
Zespół w składzie: prof. dr hab. Maria Nowakowska, dr hab. Joanna Lewandowska-Łańcucka oraz dr Adriana Gilarska opracował materiał, który pomoże odbudowywać ubytki kostne i jednocześnie może służyć jako nośnik leków przeciwko osteoporozie dostarczając je wyłącznie w miejsca zmienione chorobowo. Nowy materiał ma postać hydrożelu, który wstrzykuje się w miejsce ubytku kości, gdzie następnie dochodzi do jego „zestalenia” w wyniku sieciowania chemicznego zachodzącego w temperaturze 37°C. Ze względu na swoją strukturę i skład hydrożel trwale przyczepia się do tkanki kostnej i pełni funkcję rusztowania, na którym w naturalnych procesach biologicznych tworzy się nowa tkanka kostna wypełniająca ubytek.
Wynalazek zaprojektowany został z uwzględnieniem dodatkowej funkcji nowego materiału. Skład chemiczny hydrożelu pozwala na to, by stał się on nośnikiem leków na osteoporozę podawanych miejscowo, wyłącznie w okolice chorych tkanek i ubytków kostnych. Opracowana metoda daje dwie zasadnicze korzyści. Po pierwsze, pozwala odejść od ogólnoustrojowego podawania leków na osteoporozę, które mają silne skutki uboczne. Po drugie, hydrożel daje możliwość aplikowania znacznie większych stężeń leku w bezpośrednie sąsiedztwo chorych tkanek i tym samym zwiększenia efektywności terapii. Przy okazji, ze względu na swoje właściwości, dodatkowo pojawiają się szanse na naturalną odbudowę kości w miejscu ich ubytków.
Materiał został dotychczas przebadany na modelu mysim. Celem testów było wykazanie szeroko pojętej biokompatybilności hydrożelu w warunkach in vivo. Naukowcy dowiedli, że po wstrzyknięciu preparat nie wywołuje efektu toksycznego. Ponadto wykazano, że w miejscu podania hydrożelu zachodzi naturalna angiogeneza, czyli powstawanie włosowatych naczyń krwionośnych. To wskazuje na możliwość realnego wykorzystania tego materiału jako bazy dla odbudowujących się tkanek kostnych. Sam hydrożel także ulega naturalnej, stopniowej degradacji. Badania in vivo były prowadzone przez 60 dni i w ostatnim dniu w miejscu podania hydrożelu wciąż były widoczne jego pozostałości. Co więcej, w badaniach in vitro potwierdzono, że podany w hydrożelu lek, alendronian sodu, jest uwalniany do organizmu stopniowo, co dodatkowo może zwiększać skuteczność terapii.
Obecnie zespół naukowy poszukuje możliwości współpracy z inwestorami, którzy zaangażowaliby się w dalszy rozwój wynalazku i w niezbędne do przeprowadzenia badania kliniczne. Naukowcy nie wykluczają zarówno komercjalizacji pośredniej, na przykład poprzez założenie spółki typu spin-off, jak również realizacji kolejnych prac rozwojowych z pomocą finansową NCBR lub NCN. Wskazują, że konieczne jest ostateczne przeprowadzenie badań toksykologicznych, wykonanie testów na większych zwierzętach, jak również określenie optymalnych stężeń leku dla uzyskania optymalnych efektów terapeutycznych.
Twórcy hydrożelu obecnie pracują nad dalszymi modyfikacjami krzemionki wykorzystywanej w jego składzie, tak by zwiększyć możliwości sterowania planami leczenia osteoporozy. W optymalnym scenariuszu miejscowo podany lek jest uwalniany stopniowo, dodatkowo zwiększając efektywność terapii. Właśnie taki model działania został zaproponowany w materiale opracowanym na UJ. Wynalazek został objęty ochroną patentową na terenie Polski i poza granicami.
Serdecznie gratulujemy!

